|
|
Главная » 2010 » Февраль » 10 » Свинцово-кислотный Аккумулятор
01:38 Свинцово-кислотный Аккумулятор |
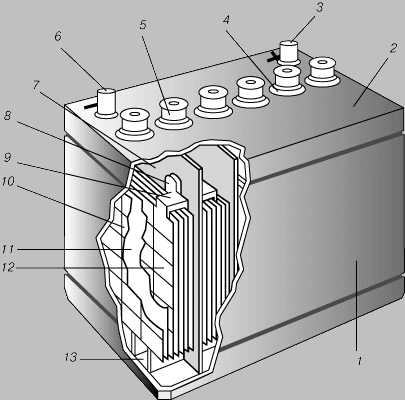 Простейший свинцово-кислотный аккумулятор состоит из положительного электрода (катод) из двуокиси свинца и отрицательного электрода (анод) из губчатого свинца РЬ, помещенных в сосуд с электролитом — 25—30-процентный водный раствор серной кислоты (H2SO4+H2O), что соответствует плотности электролита, равной 1,25—1,31 г/см3. Простейший свинцово-кислотный аккумулятор состоит из положительного электрода (катод) из двуокиси свинца и отрицательного электрода (анод) из губчатого свинца РЬ, помещенных в сосуд с электролитом — 25—30-процентный водный раствор серной кислоты (H2SO4+H2O), что соответствует плотности электролита, равной 1,25—1,31 г/см3.
Объяснение процессов, протекающих в свинцово-кислотных аккумуляторах, наиболее достоверно может быть дано общепринятой теорией двойной сульфитации. Согласно этой теории при разряде на обоих электродах происходит образование одного и того же продукта — сульфата свинца PbS04 (отсюда и название теории), вследствие восстановления двуокиси свинца а положительном электроде .и окисления губчатого свинца РЬ на отрицательном. При этом количество серной Кислоты в электролите "уменьшается, а количество воды — увеличивается и соответственно понижается плотность электролита. Процесс образования сульфата свинца прекращается, когда все активное вещество прореагирует (вся площадь обоих электродов будет покрыта сульфатом свинца). В результате ЭДС станет равна нулю. Во время заряда положительный электрод аккумулятора соединяют с положительным- полюсом источника постоянного тока, а отрицательный электрод — с отрицательным.
При прохождении зарядного тока химические процессы проходят в обратном направлении: сульфат свинца (положительного электрода превращается в двуокись свинца), сульфат свинца отрицательного электрода — в металлический свинец (РЬ) в виде рыхлой губчатой массы, в электролите увеличивается количество серной кислоты и уменьшается количество воды, следовательно, повышается его плотность. Процесс продолжается до того момента, пока весь сульфат свинца не преобразуется на обоих электродах в активные вещества. В результате ЭДС возрастет до максимальной величины.
Поскольку в обоих случаях изменяется плотность электролита, то на практике по величине плотности судят о степени заряженности аккумулятора. Так, в период разряда уменьшение плотности электролита на 0,01 г/см3 соответствует снижению емкости аккумулятора (отдаваемое аккумулятором количество электричества) на 6%.
Потенциалы электродов связаны с концентрацией электролита и для указанных выше величин его концентрации примерно равны: для отрицательного электрода—0,35 В, для положительного электрода + 1,68 В.
Таким образом, ЭДС аккумулятора будет равна £=1,68—(—0,35) =2,03 В.
|
|
Категория: Аккумуляторы |
Просмотров: 1765 |
Добавил: Serg
| Рейтинг: 0.0/0 |
Добавлять комментарии могут только зарегистрированные пользователи. [ Регистрация | Вход ] |
|
|







